ЖИТИ ДОВШЕ? СКІЛЬКИ ПОБАЖАЄТЕ!
Цією публікацією ми розпочинаємо серію матеріалів, в яких пропонуємо суспільству звернути увагу на проблеми, пов’язані зі здоров’ям людини, продовжуваністю її життя, з демографічною ситуацією та запропонувати аналіз можливостей застосування досягнень нанотехнологій для їх вирішення.
ЧОМУ САМЕ ПРО ЗВИЧКИ МОВА?
Відомо, що генетичний потенціал тривалості людського життя перевищує 150 років. Проте мало хто в світі досягає такого поважного віку, а в Украіні за останні 60 років продовжуваність життя зупинилась на 62 роках для чоловіків та 74 – для жінок, що на 15 років менше середньо європейського рівня. А причиною цього є не тільки давні та новітні хвороби, про які поговоримо згодом, але й так звані шкідливі звички самої людини. Ви вважаєте, що це не так? Тоді просимо до фактів.
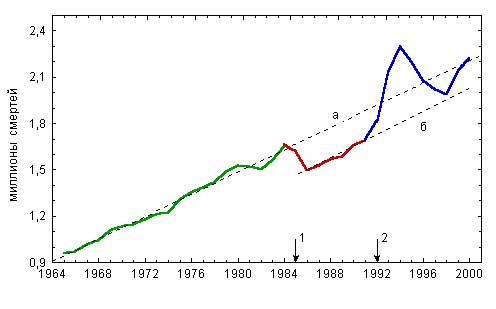
Загальна кількість смертей в СРСР 1965 – 2000 рр.
1 –початок антиалкогольної компанії; 2 – початок ринкових реформ; а – лінія регрессії для 1965-1984 рр.; б – для 1986-1991 рр.
Майже ідеальні експериментальні умови для дослідження впливу вживання алкоголю на смертність населення склалися в СРСР в результаті антиалкогольної кампанії 1986 року. Помітне зниження смертності почалося вже через 2-3 місяці після початку кампанії, а очевидне – через півтора року: на 203,5 тисячі, або на 12,3% в 1986 р. від загальної кількості смертей в 1984 році (див. графік).
Смертність від захворювань системи кровообігу, яка занизилася протягом антиалкогольної кампанії
|
Діагнози |
Доля в загальній смертності від хвороб кровообігу (1984), в % |
Зниження під час антиалкогольної кампанії, в % |
||
|
Чоловіки |
Жінки |
Чоловіки |
Жінки |
|
| Кардіосклероз атеросклеротичний без гіпертонічної хвороби |
36,2 |
37,3 |
19,4 |
21,6 |
| Судинні ураження мозку без гіпертонічної хвороби |
24,9 |
27,3 |
7,7 |
7,0 |
|
Всі інші |
38,9 |
35,4 |
6,6 |
0,0 |
|
100,0 |
100,0 |
|||
Як бачимо, смертність від захворювань системи кровообігу протягом антиалкогольної кампанії суттєво занизилася. Але, якщо у вас з’явилася думка, що зараз я запропоную ввесті в Україні сухий закон, це не так. Також як не пропоную ввесті тотальну заборону в країні тютюнопаління, яке значно підсилює негативні наслідки вживання алкоголю. Я пропоную допомогти людині подолати ці залежності медикам.
Але лавина найсучасніших лікарських препаратів не в змозі побороти не лише такі залежності – навіть жодне хронічне захворювання. Вочевидь, для задоволення потреб в якісній медицині необхідні кардинально нові підходи. Серед них сьогодні чільне місце займають технології й процеси, використовувані в медицині, що базуються на досягненнях в «світі малих форм» – нанотехнології.
КОЛИ ФАНТАСТИКА СТАЄ РЕАЛЬНІСТЮ
Ще у 1959 р. в своїй знаменитій лекції «Там знизу – багато місця» [1] знаменитий американський фізик-теоретик Річард Фейнман говорив про світ незвичайно малих розмірів і тому невидимий звичайним оком. Сьогодні ми ще далекі від описаного Фейнманом мікроробота, який здатний через кровоносну систему проникнути до серця та виконати там операцію на клапані. Але вчені вже навчилися переміщати окремі атоми і здійснювати «молекулярну хірургію» – змінювати структуру клітини на молекулярному рівні. З’явилася ціла галузь науки, що ввібрала в себе найновіші досягнення фізики, хімії і біології – нанотехнологія.
У широкий науковий вжиток цій термін був введений Ериком Дрекслером, американским вченим та популяризатором науки, в його книзі «Машини творення: прийдешня ера нанотехнології» (1986). Дрекслер передбачив, що развиток нанотехнологій зможе суттєво впливати на тривалість життя людства, його якість. Наприклад, все – від нанопосуду до нанокилимів – буде самоочищуючими, бо для цих наномашин бруд буде їжею. Інші системи зможуть навіть створювати свіжу їжу: справжнє м’ясо, зерно та овочі – прямо вдома.
Перспективи нанотехнології захопили уми вчених. Фармакологи та лікарі побачили в ній можливий якісний прорив у лікуванні хвороб, бо ця технологія дозволяє працювати з речовиною в нанометрових масштабах. Якраз ці розміри характерні для основних біологічних структур – клітин і молекул.
ОСНОВНІ НАПРЯМИ НАНОТЕХНОЛОГІЇ
У зв’язку з великою соціальною значущістю найбільш швидкими темпами розвиваються і впроваджуються нанотехнології для діагностики, моніторингу та лікування захворювань.
Вирізняють п’ять основних напрямів застосування нанотехнологій в медицині. 1. Доставляння лікарських речовин. Нещодавно це була лише мрія, а зараз адресно доставляюти лікарські речовини в клітини-мішені джерела розвитку патологічного процесу можна за допомогою наночастинок, які стають своєрідними «кур’єрами» або «контейнерами». В якості останніх можуть бути використани наночіпи – фосфоліпідні частинки, ліпосоми і фулерені [9] (див. мал.1).
Мал.1 Наночастинка, як контейнер для переносу генетичного матеріалу
Вирізняють два напрями адресної доставки ліків: пасивний направлений транспорт (полегшене подолання природних бар’єрів) та специфічна доставка (впізнавання патологічної тканини) [10].
Наприклад, речовина куркумін має потужну протиракову дію, але його практично не могли використовувати через погану розчинність у воді. Використання контейнера з наночастинок дозволило дослідникам із Індії обійти це обмеження.
Як показали дослідження американських учених, для доставці спеціалізованих засобів можливе використання бактерій.
А групою українських дослідників в складі З. Ульберг, Т. Грузіна, О. Карпов доведена можливість трансмембранного транспортування нанорозмірних комплексів і частинок у клітинах бактерій, здатних до вибіркового акумулювання колоїдних частинок золота, а також визначили молекулярні структури і механізми, відповідні за цей процес [11–12]. У досліджуваних клітинах ідентифіковано Mg-АТФ-азну активність, що складається з двох компонент: азидчутливої (63%) та азид-резистентної (37%). При цьому для виготовлення таких частинок-носіїв можна використовувати різні матеріали [13].
Є і зовсім екзотичні розробки. Проект, над яким працюють вже кілька років дослідники в Університеті штату Юта США являє собою микросубмарину з двигуном, що використовує роботу бактерій, таких як как Salmonella typhimurium.
2. Нові методи і засоби лікування на манометровому рівні. Наприклад, прицільна протипухлинна терапія для щоденного клінічного використання має включати такі елементи: – можливість молекулярного відображення найменших проявів наночастинок на клітинному рівні; – ефективний механізм молекулярного прицілювання після ідентифікації певних клітинних маркерів; – технологію знищення клітин, ідентифікованих як злоякісні; – технологію моніторингу одержаного ефекту.
Сучасний стан розвитку нанотехнологій вже дозволяє практично конструювати працездатні медичні нанороботи (мал.2), здатні усувати дефекти в організмі хворої людини шляхом керованих нанохірургічних втручань, зокрема, прилади для контролю рівня глюкози у крові та для виробництва інсуліну. Методиками молекулярного моделювання продемонстровано можливість створення на порядок більш складних систем: штучних еритроцитів і т.і.
Рис. 2. Наноробот в кровоносній системі
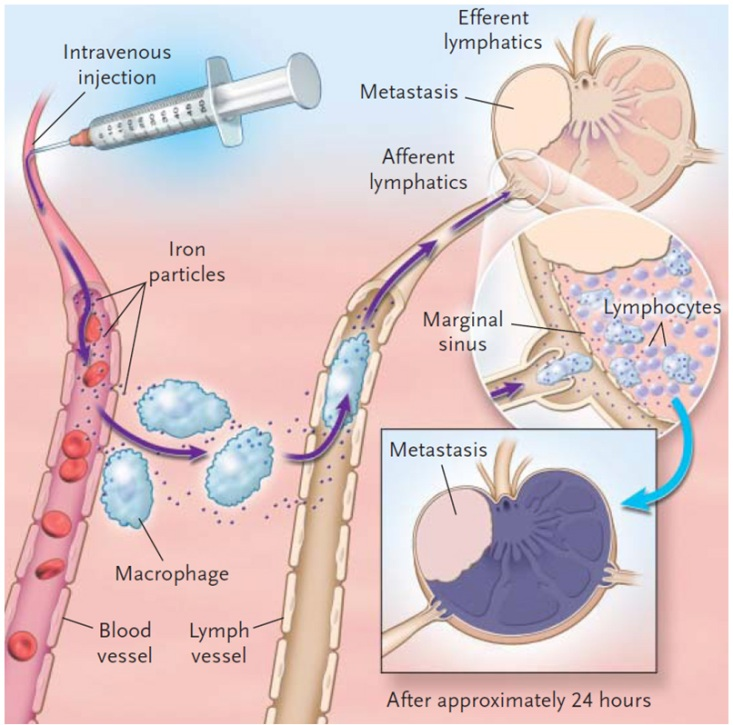
3. Діагностика in vivo. Впровадження нанотехнологічних підходів у практику медичної діагностики дозволяє здійснювати раню діагностику захворювань, виявляти онкологічні, ендокринні, серцево-судинні захворювання, вірусні та бактеріальні інфекції та покращити продуктивність діагностикі, основаної на передачі візуальної інформації про молекулярні структури – молекулярної фізіографії [14-16]. Контрастна речовина для неї складається з наночасток, з якими з’єднані компоненти, що візіалізуються, та певні антитіла, або які-небудь інші молекули, що здатні відшукати ціль. Коли контрастна речовина вводиться в кровоток, компоненти, що візіалізуються, попадають в хворі тканини. Після чого лишається «зчитати» візіалізовану інформацію (мал.3).
Мал. 3. Наночастинки дозволяють виявляти метастази в лімфовузлах
Над цією концепцією працює компанія Kereos (СтЛуис), яка в співробітництві зі світовими концернами Philips и Bristol-Myers Squibb розробляє контрастні речовини на основі наноемульсії перфтокарбона. Це майбутне, але вже зараз в медичної практиці використовуються прості контрастні речовини торгівельної марки Resovist® компанія Schering, які складаються з наночасточок окису заліза.
4. Діагностика in vitro розвивається в двох напрямках: – використання наночасток як маркерів біологічних молекул; – застосування іноваційних нанотехнологічних способів вимірювання. Фірма Nanosphere із Іллинойса розробила нові діагностичні тести для виявлення онкологічних захворювань, хвороби Альцгеймера та муковісцідоза. При цьому заявлено, що останній буде коштувати в 10 разів дешевше теперішніх.
А сенсорні системи Cantilever и SPR вже зараз широко використовуються в медицині. Перша суттєво спрощує діагностику. Друга дозволяє вимірювати взаємодію між протеїнами або між протеїнами і ДНК в режимі реального часу.
Варто згадати ще діагностичну систему Quicklab, розроблену Інститутом кремниевих технологій (ФРН) та реалізовану концерном Siemens Corp. Technology, для експресдіагностики інфекційних захворювань, зараження крові, запалення легень, інших хвороб, де молекули ДНК та протеїни визначаються біохімічним методом.
5. Медична імплантація отримала в останне десятиліття імпульс для розвитку в зв’язку з необхідністю в способах і засобах відновлення чи заміщення органів та тканин.
Ціла низка фірм вже давно працюють з нанокристалічними матеріалами і покриттям поверхні імплантатів гидроксилопатитом для лікування кісткових дефектів. Завдяки нанокристалічній структурі поверхні імпланта процес остеогенеза практично включає штучний матеріал в природну кістку.
Іншим методом є нанокристалічне алмазне покриття, яке також обіцяє значно подовжити функціонування і стабільність імплантатів.
Нещодавно почав розвиватися ще один напрямок створення біоматеріалів – нановолокон, котрі вчені хочуть використати при тканинному інженірінзі, – створенні штучних тканин (в перспективі, – органів) на основі клітинних технологій. Визначають також наступні пріоритети розвитку нанотехнології: – супершвидкісні молекулярні детектори для визначення первинної структури генома на основі неорганічних нанопор; – геноми, які саморозмножуються, що застосовуються з метою виробництва ліків, проведення фармакологічного скрінінгу і моделювання патологічних процесів; – біосумістні наноматеріали широкого спектру застосування для створення принципово нових типів перев’язочних матеріалів та штучних органів. Вже розроблена методика відтворення хрящової тканини, яка має механічні та біохімічні властивості, близькі до природнього хряща, для відновлення механічних властивостей зубної емалі; ведуться розробки у створенні технології обробці поверхонь методом нанонапилення з метою надання їм антибактеріальних властивостей.
Таким чином, нанотехнології є мультидисциплінарним напрямом фундаментальної та прикладної науки з широким спектром різноманітних засобів та інструментів на стику інженерії, біології, фізики та хімії. Їх розвиток випереджає найсміливіші прогнози теоретиків відносно як і найяскравішого так і найбільш похмурого майбутнього всього людства в результаті широкого використання нанотехнологій в нашому житті.
УКРАЇНА ТА НАНОТЕХНОЛОГІЇ В Україні, для виконання передових досліджень і розробок в області наномедицини та нанобіотехнологій, спрямованих на створення інноваційних лікарських препаратів і систем діагностики з приватної ініціативи за підтримки президента Національної академії наук України академіка Б.Є. Патона створено ТОВ «НаноМедТех».
Наведені малюнки 4-7 – це зображення, отримані за допомогою електронного скануючого мікроскопу Mira 3 Tescan ТОВ «НаноМедТех».
За період своєї роботи вітчизняні вчені наблизились до створення функціональних наночастинок, що дасть змогу використовувати їх для діагностики захворювань, адресної доставки та контрольованого вивільнення лікарських препаратів, терапії.
Наприклад, наночастинки срібла (мал. 4.) проявляють антивірусні, антибактеріальні та ранозагоювальні ефекти, золота – протизапальні, а наночастинки CeO2 мають яскраво виражені антиоксидантні, корегуючи та регенеративні властивості.
На основі наночастинок срібла вже розробляють нанодезінфектанти. Вони мають широкий спектр біоцидної і антивірусної активності та більш високу токсичність стосовно до мікробів, вірусів і грибків, у тому числі до штамів, які вже не сприйнятливі до традиційних антибіотиків, дезінфектантів та антисептиків. Наприклад, папір з нанесеним на нього наночастинками срібла (мал. 5) володіє згубними властивостями для таких бактерій, як кишкова паличка.
Завдяки новітнім технологіям отримання та нанесення наночастинок можна досягти рівномірного розподілу наночастинок по поверхні паперу та уникнути утворення агломератів (мал. 6), що призводить до збільшення ефективної поверхні срібла при зовсім невеликої витраті металу. Також, нанесення наночастинок срібла на сульфаніламід (стрептоцид) (мал. 7), який сам по собі володіє широким спектром протимікробної дії, модифікує існуючий лікарський засіб та призводить до таких позитивних ефектів як пролонгація та локалізація дії.
Мал. 4 Наночастиники срібла синтезовані хімічним методом
Мал. 5 Волокна паперу з нанесеними на них наночастинками срібла (при такому збільшенні наночастинки ледь помітні у вигляді білих цяток на волокнах паперу).
 Мал. 6 Наночастинки срібла на поверхні волокон паперу.
Мал. 6 Наночастинки срібла на поверхні волокон паперу.
Мал. 7. Сульфаніламід, поверхня якого вкрита наночастинками срібла.
* * * Ми повинни признати, що успіхи та досягнення традиційної медицини не супроводжуються радикальним покращенням здоров’я населення. Всі тенденції ведуть до того, що саме наномедицина може стати тією галуззю, яка буде суттєвою віхою у розвитку людства. Саме тому уряди розвинених країн світу виділяють значні кошти на фінансування нових розробок лікарських препаратівтна базі нанотехн.
Узагальнюючи інформацію щодо перспектив розвитку нанотехнлогій в медицині з огляду на результати прослуханих лекцій в Стендфордському університеті півроку тому, автор цієї статті прийшов до висновку: зупинення негативного впливу шкідливих звичок на продовжуваність життя людини можливе тільки за умови поєднання досягнень традиційноі медицини та нанотехнологій.
Діденко Микола
Література:
1. Feynman R. P. There’s Plenty of Room at the Bottom // Engineering and Science (California Institute of Tech-nology). – 1960. – P. 22- 36.
2. Liu W.T. Nanoparticles and their biological and environmental application // J. Biosci. Biomed. — 2006. — №102. — P. 1–7.
3. Овчаренко Ф.Д., Эстрела-Льопис В.Р., Гаврилюк А.И., Духин А.С. О силах взаимодействия микроорганизмов и минеральных частиц в природных дисперсных системах // Физико-химическая механика и лиофильность дисперсных систем – К.:Наукова Думка, 1985. – Вып. 17. – С. 3–14.
4. Ульберг З.Р., Грузина Т.Г., Перцов Н.В. Коллоидно-химические свойства биологических наносистем.Биомембраны // Коллоидно-химические основы нанонауки. — К.: Академпериодика, 2005. — С. 199–237.
5. Estrela-Llopis V.R. The phenomenology of the vital activity for biocolloids (microorganisms) from the colloid science viewpoint // XII International Conference Surface Forces, Zvenigorod (Russia). -2002.- Р. 35.
6. Коллоидно-химический механизм связывания металлов микроорганизмами // Коллоидный журнал. — 1994 — Вып. 58. — №4. — С. 584–588.
7. Ulberg Z.R., Dukhin A.S., Karamushka V.I. Interaction of energized bacteria cells with particles of colloidal gold: peculiarities of the process // Biochimica et Biophysion Acta. — 1992. — №1134. — Р. 89–95.
8. Ulberg Z.R., Karamushka V.I., Dukhin A.S. ATR — Dependent Gold Accumulation by Living Chlorella Cells // Acta Biotechnologica. — 1991. — Vol. 11. —№3. — Р. 197–203.
9. Gregoriadis G. – Engineering liposomes for drug delivery: progress and problems // Trends Bio technol. — 1995. — №13. — Р. 527–537.
10. Roy I., Ohulchaskiy T.Y., Pudavar H.E., Bergey E.Y.,Oseroff A.R., Morgan J., Dougherty T.J., Prasad – P.N. Ceramic-based nanoparticles entrapping water insoluble photosensitizing anticancer drugs: a novel drug-carrier system for photodynamic therapy// J. Am. Chem. Soc. — 2003. — №125. — Р. 7860–7865. 13. Qu L.H., Peng X.G. Control of photoluminescenceproperties of CdSe nanocrystals in growth // J. Am.Chem. Soc. — 2002. — №124. — Р. 2045–2055.
11. Ульберг З.Р., Карамушка В.И., Грузина Т.Г. Определение локализации и выделения фактора, связывающего коллоидные частицы золота // Биотехнология. — 1986. — №1. — С. 65–68.
12. Данилович Г.В., Грузіна Т.Г., Ульберг З.Р., Костерін С.О. Ідентифікація та каталітичні властивості Mg+2 — залежної АТР-гідролази плазматичних мембран Bacillus sp B 4253, здатних до накопичення золота // Укр. біохім. журнал. — 2004. — №16. — С. 45–51
13. Данилович Г.В., Грузіна Т.Г., Ульберг З.Р., Костерін С.О. Вплив іонного та колоїдного золота на АТР-гідролазні ферментні системи в мембрані мікроорганізмів Bacillus sp B4253 та Bacillus spВ4851 // Укр. біохім. журнал. — 2007. — №77. —С. 82–87.
14. Gao X., Cui Y., Levenson R.M., Chung L.W.K., Nie S. – In vivo cancer targeting and imaging with semiconductor quantum dots // Nat. Biotechnol. —2004. — №22. — Р. 969–976
15. Ito A., Shinkai M., Honda H., Kobayashi T. – Medical application of functionalized magnetic nanoparticles // J. Biosci. Bioeng. — 2005. — №100. — Р. 1–11.
16. Harisinghani M.G., Barentsz J., Hahn P. F. et al. – Noninvasive detection of clinically occult lymphnode metastases in prostate cancer // N. Engl. J. Med. 2003. V. 348, №25. P. 2491–2499.

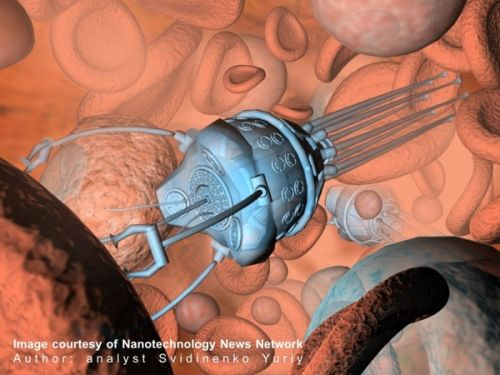



Сучасний стан розвитку науки і техніки НЕ дозволяє практично конструювати працездатні медичні нанороботи, як на мал.2. І ще не скоро дозволить, якщо взагалі колись дозволить.
До пори до часу думаю так і буде. Але рано чи пізно до цього людство дійде.